Ферментативные реакции.
Распад
глюкозы до пирувата также можно разделить
на два этапа. Первый этап
(глюкоза глицеральдегидфосфат)
требует энергии в форме АТФ (2 АТФ).
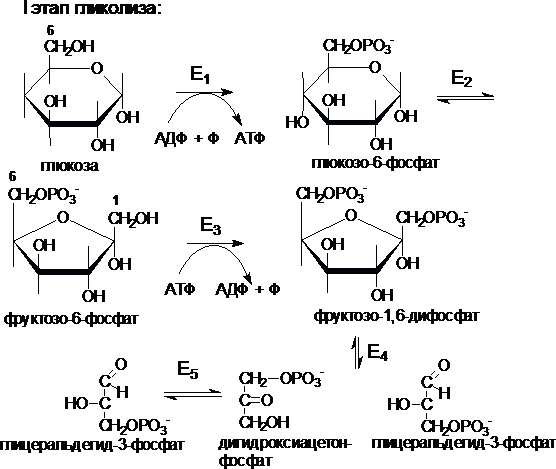
Е1 — гексокиназа или глюкокиназа
Е2 — глюкозофосфатизомераза
Е3 — фосфофруктокиназа
Е4 — фруктозодифосфатальдолаза
Е5 — триозфосфатизомераза
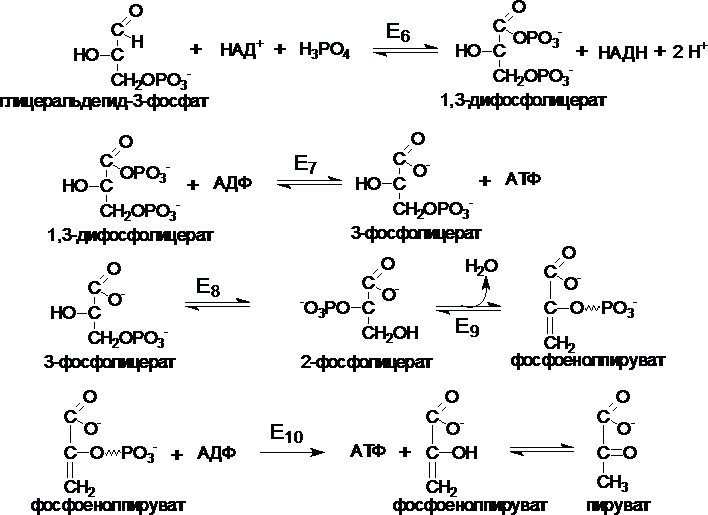
Второй
этап (глицеральдегид пируват)
протекает с выходом энергии в виде АТФ
и НАДН (4 АТФ и 2 НАДН).
Е6 — глицеральдегид-3-фофатдегидрогеназа
Е7 — фосфоглицераткиназа
Е8 — фосфоглицератфосфомутаза
Е9 — енолгидратаза
Е10 —
прируваткиназа
Особенности
ферментов гликолиза.
На
пути гликолиза три реакции являются
необратимыми (реакция 1 —глюкокиназная, реакция
3 — фофофруктокиназная, реакция
10 —пируваткиназная).
Они катализируются регуляторными
ферментами и определяют скорость всего
процесса гликолиза. Кроме того, именно
эти реакции отличаются от реакций
обратного пути — синтеза глюкозы
(глюконеогенеза).
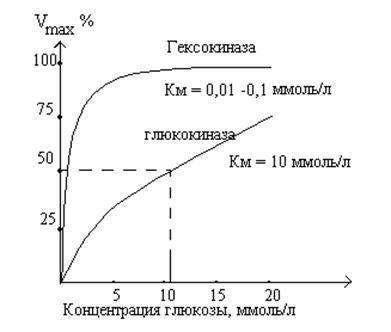
Гексокиназа
и глюкокиназа
Глюкокиназная
реакция — первая АТФ-зависимая реакция
гликолиза. Она катализируется
тканеспецифическими ферментами
— гексокиназами.У
человека известно 4 изомера гексокиназ
(типы I — IV).
Изофермент IV типа
— глюкокиназа. Глюкокиназа находится
только в печени и имеет высокое значение
Км к
глюкозе. Это приводит к тому, что фермент
насыщается субстратом лишь при очень
высоких концентрациях глюкозы. Гексокиназа
катализирует фосфорилирование глюкозы
при любых (в том числе низких) концентрациях
глюкозы и ингибируется продуктом
глюкозо-6-фосфатом. Глюкокиназа не
ингибируется глюкозо-6-фосфатом. При
увеличении концентрации глюкозы после
приема пищи увеличивается скорость
глюкокиназной реакции. Глюкозо-6-фосфат
не проходит через клеточные мембраны
и задерживается в клетке, поэтому больше
глюкозы задерживается в печени. Таким
образом, глюкокиназа является буфером
глюкозы в крови. В тоже время, в тканях,
энергетический обмен которых зависит
от глюкозы, локализован изофермент с
низким значением Км.
Глюкозофосфатизомераза
Фермент
имеет почти равное значение Км для
глюкозо-6-фосфата и фруктозо-6-фосфата.
Этот фермент по-другому называют
гексозофосфатизомераза. Катализирует
реакции гликолиза и глюконеогенеза.
Фосфофруктокиназа
Этот
фермент катализирует только прямую
реакцию, т.е. эта реакция гликолиза
является необратимой и определяет
скорость всего процесса.
Фруктозодифосфатальдолаза катализирует
реакции гликолиза и глюконеогенеза.
Триофосфатизомераза катализирует
равновесную реакцию, и равновесие
смещается в сторону гликолиза или
глюконеогенеза по принципу действия
масс.
Глицеральдегид-3-фосфатдегидрогеназа катализирует
реакции гликолиза и глюконеогенеза.
Фосфоглицераткиназа катализирует
обратимую реакцию (гликолиза и
глюконеогенеза). Эта реакция имеет
большое значение в эритроцитах, т.к.
образующийся 1,3-дифосфоглицерат под
действием фермента дифосфоглицератмутазы превращается
в 2,3-дифосфоглицерат (ДФГ) — регулятор
сродства Hb к
кислороду.
Фосфоглицератфосфомутазаиенолгидратаза катализируют
превращение относительно низкоэнергетической
связи в 3-фосфоглицерате в высокоэнергетическую
форму, а затем в
АТФ.
Пируваткиназа —
регуляторный фермент, который катализирует
необратимую реакцию, в которой
высокоэнергетический фосфат
фосфоенолпирувата превращается в АТФ.
Пируват
далее окисляется в митохондриях. Распад
глюкозы до пирувата протекает в
цитоплазме, поэтому существует специальный
переносчик пирувата в митохондрии по
механизму симпорта с Н+.
Образующийся НАДН также должен быть
транспортирован в митоходрии для
окисления в цепи переноса электронов.
Анаэробный гликолиз
По-видимому, при содержании кислорода ниже критического уровня преобладает анаэробный гликолиз. Как и следует ожидать, влияние кислорода в каждом конкретном случае зависит от вида плодов, степени их зрелости и температуры. У плодов авокадо и цитрусовых в атмосфере, содержащей 5 % кислорода, лежкость увеличивается вдвое.
|
Строение, локализация и общие свойства быстрых и медленных мышечных волокон. |
Многие волокна при недостатке О2 продолжают работать за счет анаэробного гликолиза; в этом случае образуется молочная кислота и создается кислородная задолженность.
Наряду с аэробным метаболизмом углеводов мозговая ткань способна к довольно интенсивному анаэробному гликолизу.
Торможение процесса фосфорилирования глюкозы задерживает использование ее тканями в качестве субстрата дыхания или анаэробного гликолиза ( стр. Все это вызывает накопление неиспользованной глюкозы в избыточном количестве в организме и приводит к развитию резко выраженной гипергликемии.
Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГГ Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту.
При максимальной активности мышц, наряду с окислением глюкозы через цикл трикарбоновых кислот в митохондриях происходит усиленный процесс анаэробного гликолиза в трубках саркоплазматической сети. При этом выделяется молочная кислота, которая диффундирует в кровь. После некоторого периода максимальной работы у млекопитающих наблюдается учащенное дыхание. Поступающий кислород расходуется на окисление через цикл трикарбоновых кислот в тканях печени некоторой части избытка молочной кислоты, образовавшейся в период максимальной мышечной активности. При этом синтезируются молекулы АТФ. Остальная часть молочной кислоты, накопившейся в крови, превращается в печени в гликоген.
Попутно следует подчеркнуть, что физиологический смысл этих особенностей ЛДГ у большинства рыб может состоять в усилении тенденции к анаэробному гликолизу при высоких температурах.
АТФ / АДФ и увеличение отношения концентраций лактат / пируват в печени и плазме крови свидетельствуют о наличии пострадиационных гемоциркуляторных сдвигов, сопровождающихся снижением аэрации тканей и усилением анаэробного гликолиза
|
Конечные этапы спиртового брожения. |
У дрожжей и у других микроорганизмов, сбраживающих глюкозу не до лак-тата, а до этанола и СО2, путь ферментативного расщепления глюкозы совпадает с описанным выше для анаэробного гликолиза на всем протяжении, за исключением этапа, катализируемого лактатде-гидрогеназой. В первой из них продукт расщепления глюкозы пируват теряет свою карбоксильную группу под действием пируватдекарбоксилазы.
В этом случае гликоген превращается в Глюкозофосфат, но затем из глюкозофосфата образуется пировиноградная кислота ( гликолиз), которая используется для синтеза АТФ в процессе аэробного дыхания или анаэробного гликолиза.
Поскольку живые организмы появились на Земле еще в то время, когда ее атмосфера была лишена кислорода, то целесообразной стала простейшая форма биологического механизма получения энергии из химических веществ — анаэробный гликолиз. Организмы, существующие в анаэробных условиях и получающие таким способом необходимую им энергию, образуют два класса. Облигатные анаэробы — более примитивный класс — объединяют относительно небольшое количество бактерий и беспозвоночных, обитают, как правило, в условиях очень пониженного содержания кислорода или же полного его отсутствия.
Из выводов его работы наибольшего внимания заслуживают установление при хронической интоксикации хромом ингибирования тиоло-вых ферментов мембран, а также ферментов аэробного гликолиза, цикла Кребса и терминального окисления, угнетение синтеза аминокислот и белков, возникновение гипоксии в результате склерозирования биологических мембран и микроцир-куляторного русла, активации ферментов анаэробного гликолиза, пентозофосфатного шунта и неспецифических фосфатаз.
Еще больше увеличивается при работе мышцы в анаэробных условиях образование молочной кислоты. Интенсивность анаэробного гликолиза при работе может возрастать почти в 1000 раз.
Гликолиз
Анаэробное превращение глюкозы локализуется в цитозоле и включает два этапа из 11 ферментативных реакций.
Первый этап гликолиза
Первый этап гликолиза – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов.
Первая реакция гликолиза сводится к превращению глюкозы в реакционно-способное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой.
Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент глюкозофосфат-изомераза). В результате образуется фруктозо-6-фосфат.
Третья реакция – фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата. Эта реакция является главной в регуляции скорости гликолиза.
В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам фруктозо-1,6-дифосфат-альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ).
Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы:
- при нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза,
- при достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров.
Второй этап гликолиза
Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Шестая реакция гликолиза (фермент глицеральдегидфосфат-дегидрогеназа) – окисление глицеральдегидфосфата и присоединение к нему фосфорной кислоты приводит к образованию макроэргического соединения 1,3-дифосфоглицериновой кислоты и НАДН.
В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи, заключенная в 1,3-дифосфоглицерате тратится на образование АТФ. Реакция получила дополнительное название – реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (от субстрата реакции) в отличие от окислительного фосфорилирования (от электрохимического градиента ионов водорода на мембране митохондрий).
Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
Девятая реакция – фермент енолаза отрывает молекулу воды от 2-фосфоглицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата.
Десятая реакция гликолиза – еще одна реакция субстратного фосфорилирования – заключается в переносе пируваткиназой макроэргического фосфата с фосфоенолпирувата на АДФ и образовании пировиноградной кислоты.
Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы
Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях
| У плода и детей первых месяцев жизни преобладает анаэробный распад глюкозы, в связи с чем концентрация молочной кислоты в крови у них выше чем у взрослых. |
| При наличии кислорода пировиноградная кислота переходит в митохондрию и превращается в ацетил-S-КоА. |
История исследования
Гликолиз первый из открытых и наиболее исследован метаболический путь. 1897 братья Ганс и Эдуард Бюхнер занимались изготовлением бесклеточной экстрактов дрожжей для терапевтического применения. Очевидно, они не могли использовать ядовитые для человека антисептики, как фенол, поэтому попытались распространен в кулинарии консервант — сахарозу. Выяснилось, что в дрожжевых экстрактах это вещество быстро зброджувалась к этиловому спирту. Так впервые установлено, что брожение может происходить вне живых клеток. В 1907 году Эдуарду Бюхнеру была присуждена Нобелевская премия по химии.
Со времени открытия внеклеточного брожения до 1940-х годов исследования реакций гликолиза было одной из основных задач биохимии. Описанием этого метаболического пути в клетках дрожжей занимались Отто Варбург, Ганс фон Эйлер-Хельпин и Артур Гарден (два последних получили Нобелевскую премию по химии 1929 года), в мышцах — Густав Эмбден и Отто Меергоф (Нобелевская премия по медицине и физиологии 1922 ). Также свой вклад в исследование гликолиза сделали Карл Нойберг, Яков Парнас, Герти и Карл Кори.
Важными «побочными» открытиями, сделанными благодаря изучению гликолиза, была разработка многих методов очистки ферментов, выяснения центральной роли АТФ и других фосфорильованих соединений в метаболизме, открытие коэнзимов, таких как НАД.
ГЛИКОЛИЗ анаэробное без участия О2
ГЛИКОЛИЗ анаэробное (без участия О2) негидролитич. расщепление углеводов в цитоплазме под действием ферментов, сопровождающееся синтезом АТФ и заканчивающееся образова-нием молочной к-ты. Гликолиз одной молекулы глюкозы м. б. выражен след. ур-нием:
Субстратами гликолиза кроме глюкозы м. б. другие моносахариды, а также полисахариды. В мышечной ткани, где основной субстрат гликолиза-гликоген, процесс начинается с р-ции I и наз. гликогенолизом. У растений субстратом для гликолиза может служить крахмал. Первые этапы гликолиза, спиртового и нек-рых. др. видов брожения сходны. Стадии, в к-рых осуществляются необратимые р-ции (II-IV), играют существ. роль в регуляции скорости гликолиза. Наиб. важный регуляторный фермент-фосфофруктокиназа, катализирующая р-цию III; ее активность ингибируется АТФ, НАДН, лимонной и жирными к-тами, стимулируется АДФ и АМФ. Р-ции II и IV катализируются соотв. гексокиназой и пируваткиназой, актив-ность к-рых регулируется адениловыми нуклеотидами, промежуточными продуктами гликолиза и цикла трикарбоновых к-т. У животных и человека в регуляции гликолиза принимают участие также гормоны.
Схема гликолиза. В одинарных рамках-субстраты гликолиза, АТФ -аденозинтрифосфат, АДФ-аденозиндифосфат, НАДН и НАД-соотв. восстановленная и окисленная формы никотинамидаде-ниндинуклеотида, Р-остаток фосфорной к-ты, ~ -высокоэргич. связь. В условиях недостаточности кислорода гликолиз-единств. процесс, поставляющий энергию для осуществления физиол. ф-ций организма. В аэробных условиях гликолиз-первая стадия окислит. превращения углеводов: в присут. О2 пировиноградная к-та может подвергаться дальше окислит. декарбоксилированию, а образующаяся уксусная к-та в виде СН3С(О)КоА (КоА-остаток кофермента А) полностью окисляться до СО2 и воды в цикле трикарбоновых к-т. Интенсивный гликолиз происходит в скелетных мышцах, где он поставляет энергию для мышечных сокращений, а также в печени, сердце, мозге животных и человека. В клетках осуществляется тонкая регуляция окислит. и анаэробного обмена. Подавление гликолиза дыханием в присут. О2 (эффект П а с т е р а) обеспечивает клетке Наиб. экономный механизм образования богатых энергией соединений. В тканях, где такой эффект отсутствует (напр., в эмбриональных и опухолевых), гликолиз протекает очень активно. В нек-рых тканях с интенсивным гликолизом наблюдается подавление тканевого дыхания (эффект Крабтри).
Гликолиз-простейшая форма биол. механизма аккумулирования энергии углеводов в АТФ. Считают, что он возник в период, когда в атмосфере Земли не было О2. При энергетически более вы-годном аэробном окислении из одной молекулы глюкозы образу-ется 38 молекул АТФ.
Процесс — окисление — глюкоза
Процесс окисления глюкозы в клетке может протекать как в анаэробных, так и в аэробных условиях.
Процесс окисления глюкозы окисью серебра или гидратом окиси меди в щелочной среде очень сложен.
Поэтому процесс окисления глюкозы состоит более чем из двух дюжин промежуточных стадий, каждая из которых осуществляется при непременном участии по меньшей мере одного фермента.
В процессе окисления глюкозы выделяется тепло, необходимое организму для совершения различной работы; кроме того, окисление обеспечивает выполнение одной из наиболее замечательных и удивительных функций, которую мы и будем изучать. Оно обеспечивает синтез другой богатой энергией молекулы — аде-нозинтрифосфата, или АТФ.
К окислительным брожениям относится еще процесс окисления глюкозы в глюконовую кислоту, также вызываемый плесневым грибком Aspergillus ni ger и некоторыми бактериями.
Таким образом, энергетические возможности процесса окисления глюкозы с участием нитрата сопоставимы с энергетическими возможностями процесса аэробного дыхания. Запасание клеткой полезной энергии при денитрификации зависит от организации электронного транспорта, свойств и локализации соответствующих редуктаз.
На схеме показано, каким образом процесс окисления жирных кислот связан с процессом окисления глюкозы и лимоннокислым циклом.
Из недавней работы по фосфорному циклу при гликолизе в мышце следует, что при отсутствии равновесия изотопа между субстратом внутри и вне клетки могут возникнуть серьезные осложнения в интерпретации данных, полученных в экспериментах с индикаторами. В классической мейергофовской схеме этого процесса, аденозинтрифосфат действует как источник энергии и донор фосфора, катализируя процесс окисления глюкозы мышцей с промежуточным образованием гексозо-и триозофосфатов.
Накопление меди в этих организмах превышает содержание в окружающей воде в тысячи раз. В организм человека и высших животных медь поступает с пищей и всасывается в верхней части кишечника. Депонируется ( откладывается) в печени, костном мозге, сером веществе головного мозга. Роль медьсодержащих соединений в организме многообразна: ускорение процесса обмена, усиление тканевого дыхания, ускорение процесса окисления глюкозы, торможение разложения гликогена в печени. Основные медьсодержащие ферменты: тирозиназа, лактаза, аскор-биноксидаза, церулоплазмин гемо — и гепатокупреины в крови. Под влиянием меди активируются каталаза, пероксидаза и повышается устойчивость гормонов гипофиза. Совместно с кальцием она принимает участие в метаболизме фосфора.
Лимонная кислота затем превращается в дикарбоновую кислоту, содержащую четыре атома углерода в молекуле, причем такое превращение проходит через шесть стадий, в двух из которых освобождается по одной молекуле двуокиси углерода. В трех последующих стадиях происходит превращение образовавшейся четырехуглеродной дикарбоновой кислоты в щавелевоуксусную. Каждая из этих стадий катализируется особыми ферментами, причем некоторые из них обеспечивают образование богатых энергией молекул. Таким образом, значительная часть из очень большого количества энергии ( 470 кДж на 1 моль СО2), высвобождающейся в процессе окисления глюкозы, становится доступной для использования в самых различных целях.
Если в электродах на основе ионоселективных мембран чувствительным элементом является мембрана с избирательной проницаемостью, то редокс-электроды проявляют нернстовскую зависимость потенциала от отношения концентраций окисленных и восстановленных частиц в анализируемом растворе. Наиболее хорошо изучена глюкозоксидазная редокс-электродная система. Глюкозоксидазу иммобилизуют на платине, пористом графите или золоте. При погружении такого электрода в раствор глюкозы его потенциал линейно зависит от логарифма концентрации в диапазоне 50 — 400 мг / 100 мл, что представляет клинический интерес, поскольку нормальный уровень глюкозы в крови равен 90 — 120 мг / 100 мл. Источником потенцио-метрического сигнала в этом случае являются реакции окисления или восстановления функциональных групп на поверхности электрода пероксидом водорода, образующимся в катализируемом глюкозоксидазой процессе окисления глюкозы.
Распространение и значение
Гликолиз является почти универсальным для всех клеточных организмов путем катаболизма глюкозы. Вероятно, он возник на ранних этапах развития жизни на Земле, еще до того, как в атмосфере накопился кислород в результате деятельности фотосинтезирующих организмов. Последовательность гликолитических реакций — чрезвычайно эволюционно консервативный путь. Ферменты, которые принимают в нем участие, проявляют высокую степень гомологии как в аминокислотной последовательности, так и трехмерной структуре у позвоночных животных, дрожжей и растений. Как показало секвенирования ДНК геномов большого количества организмов, только в некоторых архей и паразитических бактерий отсутствуют один или несколько ферментов гликолиза, несмотря на то, что сам путь сохраняется, вероятно, в модифицированном виде.
В эукариотических клетках реакции гликолиза происходят в цитозоле. В большинстве таких клеток именно этот среди других метаболических путей занимает первое место по количеству атомов углерода, которые превращаются в нем. Для таких тканей млекопитающих, как мозг (за исключением условий голодания), мозговой слой почек, сперматозоиды, а также эритроциты, в которых полностью отсутствуют митохонондрии, гликолиз является единственным источником метаболической энергии. Для мышц в условиях очень большой нагрузки гликолиз выгоден не только потому, что дает возможность получить энергию при недостатке кислорода, а еще и потому, что он происходит очень быстро и обеспечивает синтез АТФ в 10,5 раз быстрее, чем аэробная окисления органических веществ . Также от гликолиза главным образом зависят растительные ткани, специализированные на хранении крахмала (например клубни картофеля), и водные растения, такие как настурция лекарственная.
Другими путями окисления глюкозы является пентозофосфатный путь и путь Энтнера-Дудорова. Последний является заменой гликолиза в некоторых грамотрицательных и, очень редко, грамположительных бактерий и имеет много общих черт с ним ферментов.
Гликоген.
Гликоген —
главная форма запасания углеводов у
животных Гликоген запасается главным
образом в печени .
Роль гликогена как
быстро мобилизуемого энергетического
резерва очень важна в их жизнедеятельности.
Избыток углеводов, поступающих с пищей,
превращается в гликоген, который
откладывается в тканях (преимущественно
в печени и мышцах) и образует депо
углеводов, из которого организм черпает
глюкозу, необходимую для обеспечения
энергией различных процессов. Если
углеводы с пищей не поступают,
запасы гликогена (ок.
500 г) полностью истощаются через 12–18 ч.
Обеднение печени углеводами приводит
к жировому перерождению её клеток.
Регуляция синтеза и распада:
Фермен-гликогенфосфорилаза активирует
АМФ и ингибиторы АТФ и глюкозо-6-фосфатом
Гликогенсинтаза стимулируется
глюкозо-6-фосфатом
Оба фермента регулируются путем новой
модификации фосфорилированием и
дефосфорилированием.
Распад
гликоген-распад происходит в
интервалах м.у приемами пищи.
Распад
гликогена происходит при участии двух
ферментов: гликогенфосфорила-зы и
фермента Голодание
в течение 24 ч приводит практически к
полному исчезновению гликогена в клетках
печени. Однако при ритмичном питании
каждая молекула гликогена может
существовать неопределенно долго: при
отсутствии пищеварения и поступления
в ткани глюкозы молекулы гликогена
уменьшаются за счет расщепления
периферических ветвей, а после очередного
приема пищи вновь вырастают до прежних
размеров. Аналогичные процессы происходят
и в мышечной ткани, но здесь они в
значительной мере определяются режимом
мышечной работы.
Глюкозо-1-фосфат,
образующийся из гликогена, при участии
фосфоглюкомута-зы превращается в
глюкозо-6-фосфат, дальнейшая судьба
которого в печени и в мышцах различна.
В печени глюкозо-6-фосфат превращается
в глюкозу при участии глюкозо-6-фосфатазы,
глюкоза выходит в кровь и используется
в других органах и тканях. В мышцах нет
этого фермента, поэтому глюкозо-6-фосфат
используется здесь же, в мышечных
клетках, распадаясь аэробным или
анаэробным путем.
БИОСИНТЕЗ ГЛИКОГЕНА .Глюкоза,
прежде чем превратиться в гликоген,
подвергается фосфорилированию. Эта
реакция происходит с участием фермента
гексокиназы (фосфотрансферазы),
катализирующего перенос фосфорного
остатка с АТФ на глюкозу.
1.
Глюкоза+АТФ —
¾ Глюкозо-6-фосфат+АДФ.
гексокиназа
Далее
глюкозо-6-фосфат превращается в
глюкозо-1-фосфат при участии фермента
фосфоглюкомутазы.
2.
Глюкозо-6-фосфат
¬¾¾¾ Глюкозо-1-фосфат
¾¾¾
фосфоглюкомутаза
Глюкозо-1-фосфат
в присутствии фермента гликозилтрансферазы
(пирофосфорилазы) взаимодействует с
уридинтрифосфатом (УТФ) с образованием
уридиндифосфатглюкозы (УДФ-глюкозы) и
пиро-фосфата.
3.
Глюкозо-1-фосфат+УТФ ¬¾¾¾
УДФ-глюкоза+Н4Р2О7
¾¾¾
пирофосфорилаза
пирофосфaт
Затем
в присутствии особой трансферазы
(гликогенсинтетазы) и «затравочного»
количества гликогена происходит
удлинение цепочки гликогена за счет
присоединения остатков глюкозы, входящих
в состав УДФ-глюкозы.
4.
Гликоген+УДФ-глюкоза
¾ Гликоген +УДФ
(затравка)
гликоген-
синтетаза
Анаэробное окисление глюкозы
Катаболизм глюкозы без О2 идет в
анаэробном гликолизе и ПФШ (ПФП).
-
В ходе
анаэробного гликолизапроисходит
окисления 1 глюкозы до 2 молекул молочной
кислоты с образованием 2 АТФ (сначала
2 АТФ затрачиваются, затем 4 образуются).
В анаэробных условиях гликолиз является
единственным источником энергии.
Суммарное уравнение: С6Н12О6+ 2Н3РО4+ 2АДФ → 2С3Н6О3+ 2АТФ + 2Н2О. -
В ходе
ПФПиз глюкозы образуются
пентозы и НАДФН2. В ходеПФШиз глюкозы образуются только НАДФН2.
ГЛИКОЛИЗ
Гликолиз – главный путь катаболизма
глюкозы (а также фруктозы и галактозы).
Все его реакции протекают в цитозоле.
Аэробный
гликолиз— это процесс окисления
глюкозы до ПВК, протекающий в присутствии
О2.
Анаэробный
гликолиз– это процесс окисления
глюкозы до лактата, протекающий в
отсутствии О2.
Анаэробный
гликолиз отличается от аэробного только
наличием последней 11 реакции, первые
10 реакций у них общие.
Этапы
гликолиза
В любом
гликолизе можно выделить 2 этапа:
-
1 этап
подготовительный, в нем затрачивается
2 АТФ. Глюкоза фосфорилируется и
расщепляется на 2 фосфотриозы; -
2 этап,
сопряжён с синтезом АТФ. На этом этапе
фосфотриозы превращаются в ПВК. Энергия
этого этапа используется для синтеза
4 АТФ и восстановления 2НАДН2,
которые в аэробных условиях идут на
синтез 6 АТФ, а в анаэробных условиях
восстанавливают ПВК до лактата.
Энергетический
баланс гликолиза
Таким образом,
энергетический баланс аэробного
гликолиза:
8АТФ = -2АТФ +
4АТФ + 6АТФ (из 2НАДН2)
Энергетический
баланс анаэробного гликолиза:
2АТФ = -2АТФ +
4АТФ
Общие реакции
аэробного и анаэробного гликолиза
1. Гексокиназа (гексокиназа II,
АТФ: гексозо-6-фосфотрансфераза) в мышцах
фосфорилирует в основном глюкозу, меньше
– фруктозу и галактозу.Кm
Глюкокиназа(гексокиназа IV, АТФ:
глюкозо-6-фосфотрансфераза) фосфорилирует
глюкозу. Кm- 10 ммоль/л,
активна в печени, почках. Не ингибируется
глюкозо-6-ф. Индуктор инсулин. Гексокиназы
осуществляют фосфорилирование гексоз.

2.Фосфогексозоизомераза(глюкозо-6ф-фруктозо-6ф-изомераза)
осуществляет альдо-кетоизомеризацию
открытых форм гексоз.

3.Фосфофруктокиназа 1(АТФ:
фруктозо-6ф-1-фосфотрансфераза) осуществляет
фосфорилирование фруктозы-6ф. Реакция
необратима и самая медленная из всех
реакций гликолиза, определяет скорость
всего гликолиза.
Активируется:
АМФ, фруктозо-2,6-дф (мощный активатор,
образуется с участием фосфофруктокиназы
2 из фруктозы-6ф), фруктозо-6-ф, Фн.
Ингибируется:
глюкагоном, АТФ, НАДН2, цитратом,
жирными кислотами, кетоновыми телами.
Индуктор
реакции инсулин.

4.Альдолаза А(фруктозо-1,6-ф:
ДАФ-лиаза). Альдолазы действуют на
открытые формы гексоз, имеют 4 субъединицы,
образуют несколько изоформ. В большинстве
тканей содержится Альдолаза А. В печени
и почках – Альдолаза В.

5.
Фосфотриозоизомераза(ДАФ-ФГА-изомераза).

6.3-ФГА дегидрогеназа(3-ФГА: НАД+оксидоредуктаза (фосфорилирующая))
состоит из 4 субъединиц. Катализирует
образование макроэргической связи в
1,3-ФГК и восстановление НАДН2,
которые используются в аэробных условиях
для синтеза 8 (6) молекул АТФ.

7.Фосфоглицераткиназа(АТФ:
3ФГК-1-фосфотрансфераза). Осуществляет
субстратное фосфорилирование АДФ с
образованием АТФ.

В следующих
реакциях низкоэнергетический фосфоэфир
переходит в высокоэнергетический
фосфат.
8.Фосфоглицератмутаза(3-ФГК-2-ФГК-изомераза) осуществляет
перенос фосфатного остатка в ФГК из
положения 3 положение 2.

9.Енолаза(2-ФГК: гидро-лиаза)
отщепляет от 2-ФГК молекулу воды и
образует высокоэнергетическую связь
у фосфора. Ингибируется ионамиF-.

10.Пируваткиназа(АТФ:
ПВК-2-фосфотрансфераза) осуществляет
субстратное фосфорилирование АДФ с
образованием АТФ.
Активируется
фруктозо-1,6-дф, глюкозой.
Ингибируется
АТФ, НАДН2, глюкагоном, адреналином,
аланином, жирными кислотами, Ацетил-КоА.
Индуктор:
инсулин, фруктоза.

Образующаяся енольная форма ПВК затем
неферментативно переходит в более
термодинамически стабильную кетоформу.
Данная реакция является последней для
аэробного гликолиза.
Дальнейший катаболизм 2 ПВК и использование
2 НАДН2зависит от наличия О2.
Анаэробный гликолиз
Анаэробный гликолиз как один из источников энергии для мышечного сокращения играет особо важную роль в белых мышцах. Большинство скелетных мышц содержит как белые, так и красные волокна, однако есть и такие мышцы, которые состоят почти целиком из одних только красных или одних только белых волокон. У индеек мышцы крыла белые и летать они могут лишь на очень короткие расстояния. У лошади, способной к длительному непрерывному бегу, мышцы ног состоят преимущественно из красных волокон. Белые мышечные волокна, содержащие мало митохондрий, отличаются чрезвычайно высо-кой частотой сокращений. Источником АТР служит для них анаэробный гликолиз, так что работать с максимальной интенсивностью они могут лишь очень короткое время, поскольку имеющийся в них запас гликогена используется малоэффективно.
Анаэробный гликолиз происходит не в митохондриях, но зато именно там протекают последующие стадии дыхания — цикл Кребса ( называемый также циклом трикарбоновых кислот и циклом лимонной кислоты) и конечное дыхание. Эти реакции изучены до мельчайших подробностей.
Анаэробный гликолиз — примитивный и единственно возможный способ получения энергии из глюкозы облигатными анаэробами, хотя он и имеет место у факультативных анаэробов, а также характерен для типичных анаэробных клеток.
Анаэробным гликолизом называется распад глюкозы до молочной кислоты в отсутствие кислорода.
Хотя анаэробный гликолиз быстрее, чем аэробный обмен веществ, он очень неэкономичен в расходовании топлива организма. Кроме того, образующаяся при гликолизе молочная кислота накапливается в мышцах, вызывая боль, которую вы, возможно, чувствовали, пробежав несколько лестничных пролетов. Предел времени — в течение которого ваше тело может получать энергию в результате анаэробного гликолиза, меньше минуты.
Изучение анаэробного гликолиза на препарате мышечной ткани показало, что при использовании в качестве субстрата гликогена лактат не образуется, тогда как добавление глюко-зо-1 — фосфата-или глюкозы приводило к нормальному гликолизу с образованием лактата.
Последовательность реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и свойства которых достаточно известны. Заметим, что гликолиз протекает в гиало-плазме ( цитозоле) клетки.
|
Уменьшение количества доступного кислорода и интенсивности обмена у водяной черепахи в первые 3 ч пребывания под водой при 24 С ( по Джексону, 1968, видоизменено. |
Решающее значение анаэробного гликолиза для черепахи в условиях аноксии впервые ясно продемонстрировал Белкин. Он использовал в качестве метаболического яда иодацетат, действие которого проявляется главным образом на уровне триозо-фосфатдегидрогеназной реакции гликолиза. Если в условиях аноксии за выживание ответствен гликолиз, то ингибирование этого фермента путем инъекции черепахе иодацетата должно было бы резко уменьшить ее выносливость по отношению к аноксии.
|
Анаэробный гликолиз в летательной мускулатуре двукрылых. |
АТФ при анаэробном гликолизе равен нулю: два эквивалента АТФ используются гексокиназой и фосфофруктокиназой соответственно и два регенерируются фосфоглицераткиназои и пиру-ваткиназой. Поскольку на этапах фосфоглицераткиназы и пируваткиназы образуются при этом 2 моля АТФ, то в итоге чистый выход АТФ составляет в этом случае 1 моль АТФ на 1 моль глюкозы.
|
Взаимосвязь обмена веществ в скелетных мышцах и в печени. При тяжелой физической нагрузке источником энергии для скелетных мышц служит гликоген, распадающийся гликолитическим путем. В восстановительный период часть образовавшегося в мышцах лактата переносится в печень и превращается в глюкозу, которая поступает в кровь и доставляется в мышцы, где используется для восполнения запасов гликогена. |
Таким образом, анаэробный гликолиз дает дополнительное количество АТР сверх того основного количества, которое вырабатывается при аэробном окислении других субстратов энергетического обмена в цикле лимонной кислоты.
Очень интересный анализ сравнительной роли анаэробного гликолиза у крупных животных, в основе которого лежат экспериментальные наблюдения над аллигаторами и другими животными.
В последнее время выделяют аэробный гликолиз и анаэробный гликолиз.
Список источников
- biokhimija.ru
- StudFiles.net
- info-farm.ru
- www.ngpedia.ru
- cribs.me
