Катаболизм
(katabole – сбрасывание вниз, спуск) представляет комплекс химических реакций распада соединений. Для некоторых эта фаза метаболизма включает только их выведение из организма (билирубин, холестерин). Интересно, что многие стадии катаболизма представляют из себя окисление, сопровождающееся выделением свободной энергии и запасанием ее в виде макроэргических веществ и использованием в различных процессах жизнедеятельности.
Благодаря локализации ферментов разных фаз метаболизма в специфических компартментах (отсеках, органеллах) клеток противоположно направленные процессы протекают одновременно, причем многие из них взаимосвязаны: продукты катаболизма часто служат субстратами в этапах синтеза, а энергия, высвобождающаяся при распаде, необходима для реакций анаболизма и т.д. Процессы, с помощью которых обеспечивается взаимосвязь между фазами метаболизма, называются амфиболическими. Нормальная жизнедеятельность организма обеспечивается динамическим равновесием между разными фазами метаболизма (Табл. 3.1), что служит яркой иллюстрацией закона единства и борьбы противоположностей.
Основные особенности разных фаз метаболизма
| Катаболизм | Анаболизм |
| Распад
Окисление Высвобождение энергии Получение низкомолекулярных соединений из высокомолекулярных |
Синтез
Восстановление Затраты энергии Образование высокомолекулярных соединений из низкомолекулярных |
В процессе катаболизма выделяют три стадии
I – Гидролитическая (пищеварительная). На данном этапе макромолекулы (белки, нуклеиновые кислоты, сложные углеводы, липиды) распадаются путем гидролиза на свои основные строительные блоки: полипептиды до аминокислот, полисахариды до моносахаридов, нейтральные жиры до глицерола и ВЖК. Процесс может локализоваться вне (распад пищевых крупных мицелл в ЖКТ), а также протекать внутри клеток, если гидролизуются подобные структуры эндогенного происхождения. Для этой стадии практически не характерны экзергонические (с выделением энергии) реакции.
II – Специфический распад – продукты первого этапа с помощью специфических ферментов распадаются до ПВК или ацетил-КоА. Гексозы, пентозы, глицерин, гликогенные аминокислоты расщепляются до ПВК, 2-оксоглутарата, сукцината, оксалоацетата – метаболитов ЦТК. Для ВЖК и кетогенных аминокислот эта стадия завершается образованием ацетилКоА и некоторых других соединений. Часть реакций является экзергоническими, при их течении высвобождается до трети заложенной в веществах энергии.
III – Неспецифический распад представляет окончательное разрушение всех немногочисленных по химической природе продуктов II стадии до СО2, Н2О. Этот этап включает окислительное декарбоксилирование ПВК, ЦТК, сопряженные с ними биологическое окисление и окислительное фосфорилирование. Заключительная стадия катаболизма служит основным поставщиком энергии: в ходе реакций высвобождается до 2/3 от всей заложенной в соединениях энергии. Учитывая взаимосвязь между фазами метаболизма логично предположить, что анаболизм тоже включает 3 стадии, отличающиеся тем, что они идут в противоположном направлении, обычно протекают в других компартментах клетки, а часть реакций в силу их энергозависимости проходит другим путем.
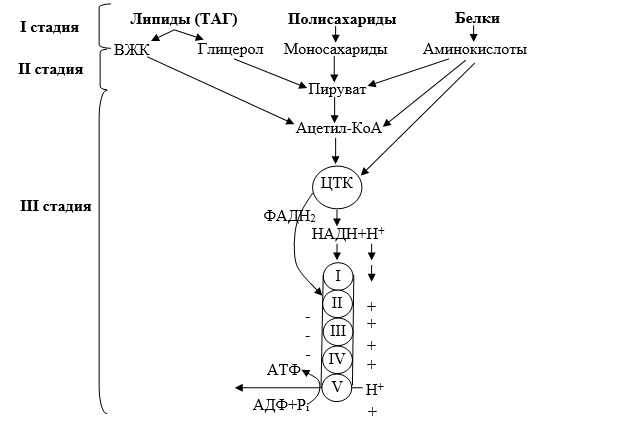
Общие и специфические пути катаболизма
В настоящее время доказано, что огромное разнообразие пищевых продуктов и в-в, из которых эти продукты состоят, при попадании в организм, подвергаются относительно ограниченным катаболитическим превращениям
Схема катаболизма Б, Л, У:
Белки Углеводы Жиры
АК Глюкоза глн. Ж.К. (моносахара)
ПВК
Ацетил КоА
ЦТК Со2
Н2о
Н+АТФ (окислительное фосфорилирование.)
1,2,3,4,5, — специфические пути катаболизма I — общий путь катаболизма.
Существует четыре этапа распада У, Ж, Б:
|
I этап — |
Распад полимеров до мономеров: Белки до АК, Углеводы домоносахаров, Липиды до жирных кислот и глицерина. Процесс распада в основ гидролитический, освобождающаяся при этом в небольшом количестве энергия превращается в тепло. |
|
II этап — |
Мономеры подвергаются дальнейшему распаду по своим специфическим путям (1, 2, 3, 4, 5, 6) в результате чего все продукты переваривания пищи превращаются в ПВКиацетил КоА. В ПВК превращаются все моносахара, глицерин, некоторые АК. Затем путем окислительного декарбоксилирования ПВК превращается в ацетил КоА. Минуяобразование ПВК в ацетил КоА превращаются жирные кислоты и некоторые АК. Далее ацетил КоА вступает в реакции окисления в лимоннокислом цикле ( цикле трикарбоновых кислот (ЦТК)) Кребса. |
Образование ацетил КоА и реакции ЦТК (I и II этапы) относятся к общему пути катаболизма. Некоторы АК вступают в общий путь катаболизма на промежуточных стадиях ЦТК.
|
III этап — |
Окисление ацетил КоА и др. метаболитов (α-кетоглутарат, щавелевоуксусная кислота (ЩУК)) в ЦТК. Этот этап сопровождается образованием восстановленных форм НАД ∙Н2 и ФАД∙Н2 |
|
IV этап — |
Через дыхательную цепь происходит перенос ℮‾от восстановленных формНАД ∙Н2 и ФАД∙Н2на кислород. В результате образуется конечный продукт Н2О. |
Не все мономеры сложных веществ пищи подвергаются катаболизмау. Часть мономеров используется для анаболических реакций, при этом синтезируются специфические для данной особи сложные вещества: Ж, Б, У, нуклеотиды и т.д.
Этот связывающий цикл, объединяющий анаболизм и катаболизм посредством энергетических системы и общих метаболитов, называется двойственным или амфиболическим путем обмена.
Окислительное декарбоксилирования ПВК и ЦТК.
Большинство тканей энергию получают за счет аэробных процессов. Полное окисление ПВК происходит через общий конечный путь обмена Ж Б У, т.е.лимонно-кислый цикл Кребса (ЦТК)в аэробных условиях.
В ЦТК включается не сам пируват, а продукт его окислительного декарбоксилирования – ацетилКоА.
ПВК предварительно путем диффузии переносится из цитозоля в митохондрии, реакция ее превращения катализируются мультиферментным пируват-ДГ-комплексом.
Общая схема реакции:
ПВК+НSКоА+НАДацетилКоА+СО2+НАД·Н2
Пируват ДГ комплекс – это мультифермент, состоящие из 3-хферментов:
а) пируват ДГ (Е1)
б) дигидролипоилтрансацетилаза (Е2)
в) дигидролипоил ДГ (Е3), в которой используют 5 коферментов:
1. тиаминпирофосфат (ТПФ),
2. амид липоевой кислоты (липоамид),
3. НSКоА,
4. ФАД,
5. НАД.
1) Реакция декарбоксилирования ПВК (ф-т Е1)
СН3СН3
| |
С=О + Е1-ТПФСН – ТПФ-Е1 + СО2
| |
СООН ОН
ПВК гидроксиэтилтиаминпирофосфат
2) Реакция окисления гидроксиэтиламинпирофосфата и перенос его на амид ЛК
СН3S
| | ЛК-Е2 ТПФ-Е1+ Н3С-С-S-ЛК-Е2
СН – ТПФ-Е1 + S || |
| окислен. форма ф-та О SН
ОН ацетиллипоат
3) Перенос ацетильной гр. на КоА (Е2)
ацетил липоатЕ2 + НSКоАНS ЛК·Е2 +СН3СО~SКоА
НS ацетил- КоА
восст. форма ферментата
4) Окисление ЛК до ее дисульфида (Е3)
НS ЛК·Е2 + Е3ФАДS
НS | ЛК Е2 + Е3ФАД·Н2
S
амид ЛК (окисл. форма).
5) Регенерация окисленной Е3ФАД· Н2:
Е3ФАД·Н2+НАДЕ3ФАД +НАД · Н2
Т.о., все ферменты дегидрогеназного комплекса оказываются в исходном положении, пригодном для следующего цикла.
Ацетил-КоАвключается в ЦТК и полностью окисляется доСО2. Когда содержание АТФ в клетке начинает превышать определенный уровень, ПДГ — комплекс, поставляющий энергетич. «топливо» для ЦТК, включается.
ПВК, является исходным субстратом общего пути катаболизма.
Энергетический обмен. Стадии катаболизма б, л, у. Источники восстановительных эквивалентов для электрон-транспортной цепи. Роль митохондрий в окислении водорода.
1 стадия.
Расщепление макромолекул на простые
субъединицы.
Пища – основной
источник Е.
Пища с Б, Ж, У попадает
в ЖКТ, далее Б → амк, У→простые сахара,
глю, Ж→ глицерин+ж.к.
2 стадия. Образование
унифицированных продуктов.
Амк(NH3)→пируват,
амк(кетогенный амин)→ацетилКоА
Глю(гликолиз)→ПВК
Глицерин+ж.к.(β-окисление)+СН3-СО-S-КоА→
ацетилКоА
3 стадия.
При полном окислении ацетилКоА до воды
и угл.газа, образуется НАДН и ФАДН, что
обеспечивает синтез АТФ в дыхательной
цепи митохондрий.
ацетилКоА→ ЦТК
+СО2
ЦТК → восстанвленный
потенциал в виде НАДН,ФАДН → траеспорт
электронов → дыхательная цепь+Н2О+АТФ
→ конечные продукты метаболизма.
Источники АТФ:
дых.цепь митохондрий(окислит.фосфорилирование),
ЦТК, β-окисление ж.к., окислительное
декарбоксилирование α-кетокислот,
гликолиз.
Источники НАДН:
ЦТК(изоцитрат-ДГ, окисл.декарб-ие
α-кетоглутарата, малатдегидрогеназа),
гликолиз(глироальдегид-3-ф-ДГ), β-окисление
ж.к. (ацетил-КоА-ДГ), окисл.декар-ие
α-кетокислот.
Источники ФАДН2:
ЦТК(сукцинат-ДГ), β-окисление ж.к.
(ацетил-КоА-ДГ), НАДН-дегидрогеназа
–вторичная флавиновая ДГ(отщепление
Н не от субстрата, а от НАДН+)
Митохондрии —
основной источник АТФ в клетке. Митохондрия
имеет две мембраны: наружную и внутреннюю.
Наружная мембрана гладкая, а внутренняя
им.крипты, содержимое митохондрии,
окруженное ее внутренней мембраной —
«матрикс митохондрии». Внутри
митохондрии имеется замкнутая в кольцо
длинная молекула ДНК и весь аппарат
синтеза белков, в том числе собственные
митохондриальные рибосомы.
Реакции цикла
Кребса происходят в жидкости, заполняющей
митохондрию, окислительное фосфорилирование
— в ее внутренней мембране.
Здесь имеется
пять типов белков дыхательной цепи,
свободно перемещающихся в пределах
этой мембраны. Их функция — медленное
поэтапное «сжигание» атомов
водорода, доставляемых переносчиками
НАД·Н и ФАД·Н2 с образованием молекул
воды. Это делается так: белок №1 отбирает
у НАД·Н электрон атома водорода и
передает его белку №2, тот — белку №3, и
так далее, до белка №5. Белки №2 и 4 имеют
небольшие размеры, поэтому в мембране
они двигаются значительно быстрее .№1,
3 и 5, по сути дела, выполняют роль курьеров,
разносящих электроны по назначению.
При этом энергия электрона все время
уменьшается. Белок №5 накапливает четыре
таких электрона, а затем производит
реакцию образования воды:4е- + О2 + 4 Н+ =2
Н2О. Энергию, выделяющуюся при прохождении
электрона по дыхательной цепи, белки №
1, 3 и 5 расходуют на выбрасывание протонов
изнутри митохондрии в пространство
между ее мембранами. В этом пространстве
создается положительный заряд, а внутри
митохондрии — отрицательный. Протоны,
накопившиеся между мембранами, в этой
ситуации имеют существенную потенциальную
энергию за счет притяжения к внутренней
части митохондрии. Во внутренней
мембране, кроме белков дыхательной
цепи, имеются молекулы еще одного белка
— АТФ-синтетазы. Они пропускают протоны
внутрь митохондрии, используя их
потенциальную энергию для синтеза АТФ.
Роль высокоэнергетических фосфатовв улавливании энергии. Клеточное дыхание
Главный путь синтеза АТФ из АДФ — окислительное фосфорилирование. При этом АДФ фосфорилируется неорганическим фосфатом:
АДФ + H3PO4 +
энергия АТФ + H2O
Реакция энергетически сопряжена с переносом водорода с
восстановительных эквивалентов на кислород. Восстановительные эквиваленты образуются
при окислении органических молекул. Последовательность реакций, с помощью которых
организм использует энергию связей органических молекул для синтеза АТФ, и при
этом углерод органических молекул превращается в углекислый газ, аводород (Н+ и е-)
переносится на молекулярный кислород с образованием молекулы воды, называется клеточным дыханием.
Другой путь синтеза АТФ из АДФ — субстратное фосфорилирование. В этом случае
макроэргическая связь в молекуле АТФ может образоваться за счет энергии
макроэргической связи в другом субстрате (например, креатинфосфате).
Таким образом, энергия пищевых веществ
в клетке трансформируется сначала в энергию АТФ, а затем АТФ служит
непосредственным источником энергии для совершения работы в биохимических и
физиологических процессах.
Механизмы регуляции цитратного цикла
Главным
и основным
регулятором ЦТК является оксалоацетат,
а точнее его доступность. Наличие
оксалоацетата вовлекает в ЦТК ацетил-SКоА
и запускает процесс.
Обычно
в клетке имеется баланс
между
образованием ацетил-SКоА
(из глюкозы, жирных кислот или аминокислот)
и количеством оксалоацетата.
Источником
оксалоацетата
является глюкоза
(синтез
из пирувата в анаплеротической
реакции),
поступление из фруктовых
кислот
самого цикла (яблочной, лимонной),
образование из аспарагиновой
кислоты
в результате трансаминирования.
-
Первая
цитратсинтазная реакция образования
цитрата из оксалоацетата и
ацетилтил-КоА
—
важнейшая регуляторная реакция всего
цикла.
Реакция активируется оксалоацетатом
— субстратом реакции, и ингибируется
продуктом — цитратом.
Увеличение энергетического потенциала
клетки (увеличение отношения
НАДН/ НАД+,
концентрация АТФ) тормозит образование
цитрата. АТФ — аллостерический ингибитор
цитратсинтазы. Его действие заключается
в повышении Км
для ацетил-КоА. Поэтому с увеличением
содержания АТФ снижается насыщение
фермента ацетил-КоА и в результате
уменьшается образование цитрата.
Ингибируют
реакцию Сукцинил-КоА и длинноцепочечные
жирные кислоты. -
Изоцитрат-дегидрогеназная
реакция аллостерически активируется
АДФ,
изоцитратом,
субстратом реакции и Са++
(3 на рис.). Фермент состоит из 8
каталитических субъединиц и при
связывании первой молекулы субстрата
в одной субъединице
за счет конформационных изменений в
других резко ускоряется присоединение
последующих молекул субстрата, что
ускоряет ферментативную реакцию
(положительный кооперативный эффект).
Фермент
аллостерически активируется АДФ и Са++,
поскольку имеет аллостери-ческие
центры связывания АДФ и Са на каждой
субъединице. НАДН
имеет более высокое сродство к
каталитическому центру фермента, чем
НАД+
и вытесняет его, что ингибирует
ферментативную активность (механизм
конкурентного
ингибирования).
3.
а-Оксоглутарат
дегидрогеназный комплекс (4 на рис.)
катализирующий преобразование
а-оксоглутарата (а-кетоглутарата) в
сукцинил-КоА, структурно подобен
и гомологичен пируват-дегидрогеназному
комплексу, но в отличие от ПДК, не
имеет регуляторных белков в своем
составе. а-Оксоглутарат дегидрогеназный
комплекс
активируется АМФ, АДФ, Са++,
но ингибируется Сукцинил-КоА, АТФ, НАДН.
АМФ,
АДФ — положительные аллостерические
регуляторы ферментативного комплекса.
Так, связывание АМФ ферментативным
комплексом уменьшает Км
для
а-кетоглутарата в 10 раз. В области
физиологических концентраций и
сукцинил-КоА
и НАДН (продукты реакции) обладают
ингибирующим эффектом, действуя по
механизму конкурентного ингибирования.
Главным регулятором активности
а-оксоглутарат дегидрогеназного
комплекса является сукцинил-КоА.
Аэробное окисление глюкозы
В аэробных
условиях глюкоза окисляется до СО2и Н2О. Суммарное уравнение:
С6Н12О6+ 6О2→ 6СО2+ 6Н2О + 2880
кДж/моль.
Этот процесс
включает несколько стадий:
-
Аэробный
гликолиз. В нем происходит окисления
1 глюкозы до 2 ПВК, с образованием 2 АТФ
(сначала 2 АТФ затрачиваются, затем 4
образуются) и 2 НАДН2; -
Превращение
2 ПВК в 2 ацетил-КоА с выделением 2 СО2и образованием 2 НАДН2; -
ЦТК.В нем происходит окисление 2 ацетил-КоА
с выделением 4 СО2, образованием
2 ГТФ (дают 2 АТФ), 6 НАДН2и 2 ФАДН2; -
Цепь
окислительного фосфорилирования.В ней происходит окисления 10 (8) НАДН2,
2 (4) ФАДН2с участием 6 О2, при
этом выделяется 6 Н2О и синтезируется
34 (32) АТФ.
В результате аэробного окисления глюкозы
образуется 38 (36) АТФ, из них: 4 АТФ в
реакциях субстратного фосфорилирования,
34 (32) АТФ в реакциях окислительного
фосфорилирования. КПД аэробного окисления
составит 65%.
Окислительное декарбоксилирование пировиноградной кислоты. Последовательность реакций. Строение пируватдекарбоксилазного комплекса.
Окислительное
декарбоксилирование пирувата происходит
в матриксе митохондрий. Транспорт
пирувата в митохондриальный матрикс
через внутреннюю мембрану митохондрий
осуществляется при участии специального
белка-переносчика по механизму симпорта
с Н+.
Превращение пирувата в ацетил-КоА
описывают следующим суммарным уравнением:
СН3-СО-СООН
+ NAD+ +
HSKoA → CH3-CO ∼SKoA
+ NADH + H+ +
CO2
В
ходе этой реакции происходит окислительное
декарбоксилирование пирувата, в
результате которого карбоксильная
группа удаляется в виде СО2,
а ацетильная группа включается в состав
ацетил- КоА. Один атом водорода оказывается
в составе NADH, а другой в виде Н+ поступает
в среду. Реакция необратима, поскольку
ΔG0′ =
-33,5 кДж/моль.
Строение
пируватдегидрогеназного комплекса
Процесс
окислительного декарбоксилирования
пирувата катализирует сложнооргани-зованный
пируватдегидрогеназный комплекс. В
пируватдегидрогеназный комплекс (ПДК)
входят 3 фермента: пируватдекарбоксилаза
(Е1),
дигидролипоилтрансацетилаза (Е2)
и дигидролипоилдегидрогеназа (Е3),
а также 5 коферментов: тиаминдифосфат
(ТДФ), липоевая кислота,. FAD, NAD+ и
КоА. Кроме того, в состав комплекса
входят регуляторные субъединицы:
протеинкиназа и фосфопротеинфосфатаза.
Все эти ферменты и коферменты объединены
в мультиферментную систему, содержащую
разные количества каждого из ферментов
и имеющую молекулярную массу более
6×106.
В центре комплекса располагается
дигидролипоилтрансацетилаза (Е2),
образуя его ядро. К дигидролипоилтрансацетилазе
присоединены молекулы: пируватдекарбоксилазы
(Е1)
и дигидролипоилдегидрогеназы (Е3).
Пируватдекарбоксилаза содержит прочно
связанный с белковой частью ТДФ, а
дигидроли-поилдегидрогеназа —
FAD.Липоиллизиновые группы центрального
фермента (Е2)
функционируют как поворотные «кронштейны»,
переносящие атомы водорода и ацетильные
группы от одной ферментной молекулы
комплекса к другой.
Окислительное
декарбоксилирование пируватаПревращение
пирувата в ацетил-КоА включает 5 стадий
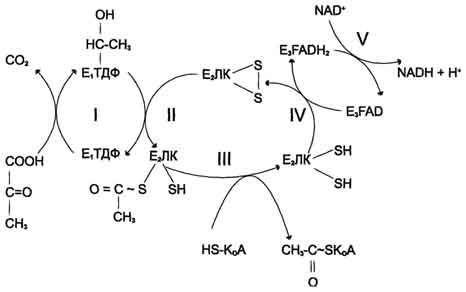
Стадия
I. На
этой стадии пируват соединяется с ТДФ
в составе Е1 и
подвергается декарбоксилированию.
Пируват
+ Е1-ТДФ
→ Гидроксиэтил-ТДФ + CO2.
-
Стадия
П. Дигидролипоилтрансацетилаза
(Е2)
катализирует перенос атома водорода
и ацетильной группы от ТДФ на окисленную
форму липоиллизиновых групп с образованием
ацетилтиоэфира липоевой кислоты. -
Стадия
III. На
стадии III КоА взаимодействует с ацетильным
производным Е2,
в результате чего образуются ацетил-КоА
и полностью восстановленный липоильный
остаток, простетическая группа Е2. -
Стадия
IV. На
стадии IV дигидролипоилде-гидрогеназа
(Е3)
катализирует перенос атомов водорода
от восстановленных липоильных групп
на FAD — простетическую группу фермента
Е3. -
Стадия
V .
На стадии V восстановленный FADH2 передаёт
водород на NAD+ с
образованием NADH.
Пируватдегидрогеназный
комплекс характеризуется большим
отрицательным окислительно-восстановительным
потенциалом, который обеспечивает
наряду с восстановлением кофермента
(NADH) образование высокоэнергетической
тиоэфирной связи в ацетил-КоА
Группы организмов по отношению к свободному кислороду
Организмы делятся на три группы:
- аэробы (облигатные аэробы) — организмы, способные жить только в кислородной среде (животные, растения, некоторые бактерии и грибы);
- анаэробы (облигатные анаэробы) — организмы, неспособные жить в кислородной среде (некоторые бактерии);
- факультативные формы (факультативные анаэробы) — организмы, способные жить как в присутствии кислорода, так и без него (некоторые бактерии и грибы).
У облигатных аэробов и факультативных анаэробов в присутствии кислорода катаболизм протекает в три этапа: подготовительный; бескислородный; кислородный. В результате органические вещества распадаются до неорганических соединений. У облигатных и факультативных анаэробов при недостатке кислорода катаболизм протекает в два первых этапа: подготовительный и бескислородный. В результате образуются промежуточные органические соединения, еще богатые энергией.
Список источников
- StudFiles.net
- xn—-7sbebdhha8f6b8b2c7a.xn--p1ai
- trotted.narod.ru
- jbio.ru
- alexmed.info
